疫苗作为一类抵御人类多种疾病,特别是传染性疾病的强大武器,它的发展逻辑同样是围绕安全性、有效性和可及性来展开。本文梳理了新冠病毒疫苗的研发及其背后的技术发展。中美两国的小型生物技术公司在新锐的疫苗开发技术的加持下,跑在了这个队伍前列。衷心希望Moderna和康希诺的临床试验进展顺利,为抗疫助力!
撰文 |Enron Medicine2020年3月16日,来自美国的Moderna公司生产的新冠疫苗mRNA-1273完成了首次人体接种试验,而mRNA-1273也成为了世界上最快的进入临床并实施接种的新冠病毒疫苗品种。紧接着在3月17日,国内的疫苗研发企业康希诺联合军事科学院陈薇院士团队研发的重组新冠病毒疫苗Ad5-nCoV也宣布进入临床试验,试验时间从2020年3月16日到2020年12月31日。在这场人类与病毒竞赛的新冠病毒疫苗研发中,中美两国得益于新锐的疫苗开发技术平台,双双进入疫苗开发的头等位置,着实让人期待又振奋。

疫苗作为一类抵御人类多种疾病,特别是传染性疾病的强大武器,它的发展逻辑同样是围绕着三大主题(即安全性、有效性和可及性)来展开的。自从1796年英国医生Edward Jenner使用牛痘病毒来给人接种从而预防天花病毒感染以来,疫苗的开发经历了200多年的发展,如今各种新技术仍然层出不穷。今天,我们就来盘点一下新冠病毒疫苗的研发及其背后的技术发展。表1. 新冠病毒疫苗的开发企业(部分)
疫苗类型
研发企业(部分)
灭活(减活)疫苗
北京科兴
Codagenix/Serum Institute of India
重组亚单位疫苗
智飞生物/中国科学院微生物研究所,三叶草生物
赛诺菲、康乐卫士、Vaxil Bio、Generex/EpiVax、昆士兰大学、Novavax
病毒载体疫苗
康希诺/军事科学院、强生、Vaxart
DNA疫苗
Inovio,Zydus Cadila
mRNA疫苗
Moderna
CureVac AG
冠昊生物/ZY therapeutic
Arcturus Therapeutics
斯微生物
BioNTech SE
灭活(减活)疫苗:保持较高免疫原性上文提到的人类最早的预防天花病毒感染的牛痘病毒就是从牛身上分离出来的活疫苗,由于它具有与人类天花病毒相同的抗原性质且对人的致病性很弱,因此在接种牛痘病毒之后,人体内可以产生抗天花病毒的抗体从而起到保护作用。

▲詹纳接受牛痘疫苗防治天花(来源:密歇根大学)然而这类活疫苗最大的特点就是它仍然保留病毒的各种特性,因此安全性不高。比如这种牛痘病毒对于正常人来说可能只是出现一些轻微的感染症状,而对于那些免疫功能缺陷患者而言,它的感染却可以是致命的。因此,为了扩大疫苗的接种范围并提高它的安全性,减活的或灭活的病毒疫苗就应运而生。病毒的灭活可以通过一些化学的(如甲醛)或物理的(如热,紫外线等)手段使得病毒失去复制能力和致病能力。而获得减活的病毒的方式是在体内或体外,在一定的条件下(如低温)不断的传代培养,这种方法可以培育出致病性低,但仍然保持较高的免疫原性的减活病毒疫苗。随着基因重组技术的发展,如今可以通过基因编辑技术将病毒中某些与病毒的复制能力和致病能力相关的基因进行修饰从而降低病毒的毒力。如我们可以将流感病毒中解码血凝素蛋白的基因进行修饰,使得解码出的血凝素是通过胰弹性蛋白酶而不是类胰蛋白酶丝氨酸蛋白酶来裂解,从而极大的降低病毒的复制能力。目前,开发灭活(或减活)新冠病毒疫苗的有北京科兴和Codagenix等企业。北京科兴成立于2001年,成立不到2年的时间就遇上了SARS病毒的肆虐,在国家科技部的牵头下,北京科兴与中国医学科学院实验动物研究所、中国疾病预防控制中心病毒病预防控制所等单位组成了疫苗研制课题组,他们历时8个月的时间成功研制出了用甲醛灭活的SARS病毒疫苗并在2004年1月进入了临床试验,然而这个时候SARS疫情已经结束,因此疫苗研发也就戛然而止。这回新冠病毒疫苗,科兴也承担了灭活疫苗的研发工作,目前尚没有最新的进展消息。重组亚单位疫苗:添加佐剂刺激免疫反应虽然基于全细胞结构的灭活或减活的病毒疫苗取得了巨大的成功,然而它的缺点也很多,首先它需要处理高活性的病毒毒株,因此需要在特定规格的实验室才能开展研制工作,比如灭活的SARS病毒疫苗的生产就需要在P3实验室里进行。再者,由于是全细胞结构,其抗原成分多样,因此它引起的人体免疫反应也更为复杂和强烈。为了解决这些问题,人们把病原体上一些可以引起人体特异性免疫反应的亚单位制备成疫苗,从而避免了病毒的复制能力和其他病原体的结构引起的不需要的免疫反应带来的副作用,极大提升了疫苗的安全性。最早这类疫苗需要从康复者血浆中分离并纯化出这些亚单元(如默沙东于1981年研发的血源性HBV疫苗Heptavax-B),这个工艺最大的问题就是疫苗的来源无法得到保证。在1986年,默沙东利用基因重组技术,将编码HBsAg的DNA整和进酵母质粒中,而后在酵母菌中表达出这些HBV的S抗原,最后经历复杂的纯化过程制备得到了人类首个用基因工程技术疫苗Recombivax HB。然而,这些高纯度的亚基单元疫苗也有一个缺点就是由于缺乏很多病原体的内在病原性特点而导致它们的免疫源性普遍不高,从而导致在体内很难引起特异性的免疫反应。因此,这类疫苗需要添加一些佐剂(如氢氧化铝等)来刺激人体的免疫反应,从而提高人体对这类亚单位疫苗的响应能力。目前,宣布开发重组亚单位新冠病毒疫苗的企业和机构有很多,国内的有智飞生物、三叶草生物等,国外的有赛诺菲,昆士兰大学,Novavax等。上面我们提到亚单位疫苗的免疫原型的缺失是因为它失去了就很多病原性的特征,如这些亚单位的结构在结构和构象上失真就是一个方面。因此,目前有很多新技术来模拟原始的病原体蛋白结构从而增加亚单元疫苗的免疫原性。三叶草生物则利用其独有的Trimer-Tag技术平台制备出了三聚体的新冠病毒S蛋白疫苗,因为在体内新冠病毒的S蛋白通常是以三聚体的形式与宿主细胞相互作用的,因此这样制备出来的三聚体S蛋白理论上有更好的免疫原性。而来自澳大利亚的昆士兰大学则利用所谓的分子钳技术(Molecular Clamp)来制备新冠病毒的S蛋白,它们利用一种称为分子钳的多肽来稳定利用基因重组技术而表达出来的新冠病毒S蛋白,从而使得这种嵌合蛋白更加容易被人体的免疫系统所识别。病毒载体疫苗:免疫原性更丰富和强烈重组的亚单位疫苗通过直接将病原体的亚单位输入人体内而引起人体的免疫反应,这样的方式一般免疫原性不高且只能引起人体的血液免疫反应。因此为了能够同时引起人体的血液免疫和细胞免疫过程从而提高疫苗的免疫原性,人们开发了几类直接在人体内产生病原体抗原蛋白的技术平台,包括重组病毒载体疫苗和核酸疫苗(DNA疫苗和mRNA疫苗)。这类疫苗的优势在于,相比于每次只能输入一次亚单位抗原,这类技术直接在体内产生抗原的时间更为长久;合成出的抗体可以分泌出宿主细胞外而引起血液免疫或者被MHC-I分子提呈而引起细胞免疫反应;表达出的抗原分子可以是多种类型而且整个过程类似于病原体的自然感染过程,因此这类疫苗的免疫原性更为丰富和强烈。目前用作疫苗载体的病毒包括腺病毒(双链DNA病毒)、甲病毒(单链RNA病毒)、痘病毒(双链DNA病毒)和疱疹病毒(双链DNA病毒)等。将编码病原体的亚单位基因整和进这些病毒的基因组后,在合适的细胞载体下扩增病毒,最后经历纯化而重组病毒载体疫苗,这类疫苗由于本身带有免疫原性的病毒载体,因此可以不需要佐剂就可以在体内引起特异性的免疫反应。
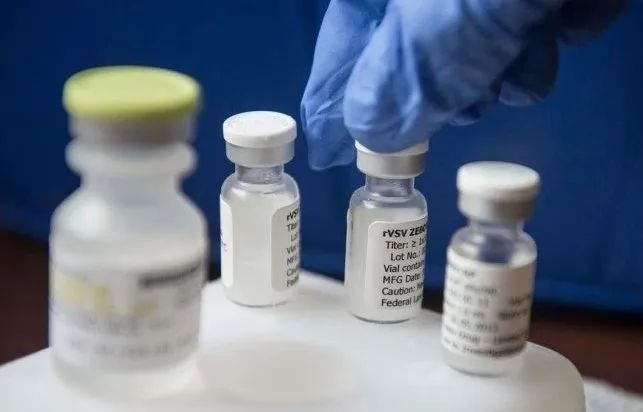
▲EBOV疫苗在2017年获批 (来源:viralportal.net)利用这类技术走在最前面的是来自国内的康希诺和军事科学院联合研制的基于复制缺陷性腺病毒为载体的Ad5-nCoV,它可以在体内表达新冠病毒的S蛋白,从而引起体内的免疫反应,目前这款疫苗已经接种了一批志愿者来评估它的安全性。值得一提的是,2017年康希诺和军事科学院利用同样的技术研发出来的艾博拉病毒疫苗Ad5-EBOV获得了国家药监局的批准上市,这也是世界上首个被国家机构批准的EBOV疫苗。这一次,他们又走在了新冠病毒疫苗的研发前列,着实令国人骄傲。DNA疫苗:合成工艺简单DNA疫苗就是将编码病原体抗原蛋白的基因整合进质粒中,而后在酵母或或其他细胞内扩增培养,而后提取纯化得到含有目前抗原的重组DNA质粒。这类疫苗的合成工艺简单,而且质粒DNA在室温下比较稳定的特点也增加了它的可及性。然而由于是外源性DNA,这类疫苗会引起抗DNA抗体,且有插入宿主细胞基因组的风险。还有一个缺陷就是这类疫苗的免疫原性不高,因此这类疫苗会添加一些佐剂,或者是在质粒DNA中引入IL-4和NF-κB p65等基因性佐剂来刺激人体的免疫反应。 ▲INO-4800预计4月进入临床试验(来源:haberdar.com)针对新冠病毒DNA疫苗开发最为迅速的是来自美国的Inovio生产的INO-4800,它正在进行临床前的测试并预计4月份进入临床试验。需要注意的是,这类疫苗除了在动物身上成功运用之外(如第一个DNA疫苗是用于马来预防西尼罗河病毒感染),目前尚没有DNA疫苗获准在人身上使用。mRNA疫苗:大大缩短流程mRNA疫苗相比于DNA疫苗的优点在于它只需要在细胞质内就可以翻译出目标抗原,因此没有整合进宿主细胞基因组的风险。然而mRNA疫苗起初并没有引起人们的广泛关注,主要原因是相比于DNA疫苗而言,它的稳定性更差,而且缺乏有效的体内递送系统。然而近些年这个领域发展速度十分迅猛,目前已有很多mRNA疫苗进入了临床试验。在mRNA稳定性方面,人们可以在mRNA中引入5-Cap和Poly-A尾部,或提升整个序列的G:C比例等手段提升它的稳定性。在体内的递送系统方面,人们开发了多种阳离子纳米乳液、阳离子多聚物脂质体和多糖颗粒等高分子递送系统,这些手段不仅可以使得mRNA更加稳定,而且可以增加它进入细胞内的能力。mRNA只需要重组酶、三磷酸核糖核苷酸和DNA模板就可以在体外的反应器中合成出来,而后经过纯化和组装进递送系统就完成了整个mRNA疫苗的生产。根据这个流程,理论上可以在很短的时间内生产出任何给定的蛋白抗原,因此这类疫苗很适合用来应对那些突然爆发的感染性疾病。
▲INO-4800预计4月进入临床试验(来源:haberdar.com)针对新冠病毒DNA疫苗开发最为迅速的是来自美国的Inovio生产的INO-4800,它正在进行临床前的测试并预计4月份进入临床试验。需要注意的是,这类疫苗除了在动物身上成功运用之外(如第一个DNA疫苗是用于马来预防西尼罗河病毒感染),目前尚没有DNA疫苗获准在人身上使用。mRNA疫苗:大大缩短流程mRNA疫苗相比于DNA疫苗的优点在于它只需要在细胞质内就可以翻译出目标抗原,因此没有整合进宿主细胞基因组的风险。然而mRNA疫苗起初并没有引起人们的广泛关注,主要原因是相比于DNA疫苗而言,它的稳定性更差,而且缺乏有效的体内递送系统。然而近些年这个领域发展速度十分迅猛,目前已有很多mRNA疫苗进入了临床试验。在mRNA稳定性方面,人们可以在mRNA中引入5-Cap和Poly-A尾部,或提升整个序列的G:C比例等手段提升它的稳定性。在体内的递送系统方面,人们开发了多种阳离子纳米乳液、阳离子多聚物脂质体和多糖颗粒等高分子递送系统,这些手段不仅可以使得mRNA更加稳定,而且可以增加它进入细胞内的能力。mRNA只需要重组酶、三磷酸核糖核苷酸和DNA模板就可以在体外的反应器中合成出来,而后经过纯化和组装进递送系统就完成了整个mRNA疫苗的生产。根据这个流程,理论上可以在很短的时间内生产出任何给定的蛋白抗原,因此这类疫苗很适合用来应对那些突然爆发的感染性疾病。
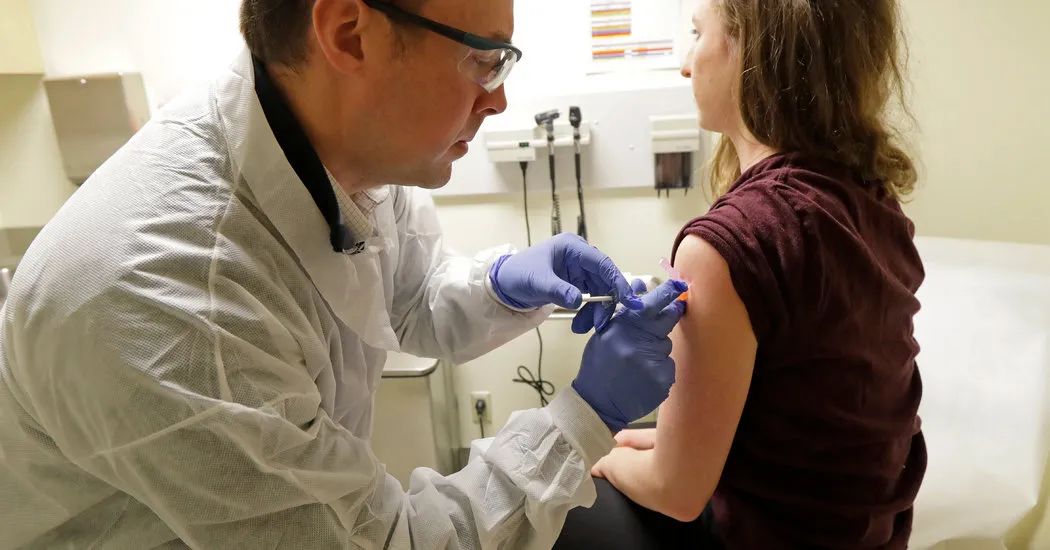
▲Moderna的mRNA疫苗进入临床试验(来源:亚特兰大商业系统)目前,Moderna是这场新冠病毒mRNA疫苗研发中的佼佼者,它旗下的mRNA-1273已进入了临床试验并完成了首例人体试验接种。此外还有来自德国的CureVac AG和BioNTech SE也处于前列。国内在这个领域最快的是斯微生物,目前正在动物模型上评估疫苗的有效性,预计今年4月份进入临床试验。当下,新冠疫情在国内基本控制住了,而国外却有愈演愈烈的趋势,截至2020年3月26日17点,国外累积确诊近40.7375万人,死亡18,854人。WHO总干事谭德塞称欧洲现在已成为新冠肺炎这一大流行病的疫情中心,目前尚无法确定这一大流行病在全球何时达到顶峰。在这样的大背景下,新冠病毒疫苗的研制工作显得尤为重要。中美两国的小型生物技术公司在新锐的疫苗开发技术的加持下,跑在了这个队伍的前列。传统的疫苗生产工艺,尤其是重组亚单位疫苗的技术工艺极为复杂,行业壁垒很高,这些技术都掌握在欧美一些大型的制药企业手里(如默沙东、GKS、赛诺菲等)。面对这场突如其来的新冠疫情,小型生物技术企业利用先进的技术来抢得疫苗研发的头等位置,从而实现弯道超车,令人鼓舞。在此希望Moderna和康希诺的临床试验进展顺利,为抗疫助力! 3月20日参考文献
1.Biotechnologyand Bioengineering. 2012, 109, 1443 - 1460.
2.Advances in Delivery Science andTechnology. Springer Science+Business Media, 2015.
3.The Journal of Infectious Diseases.2019; 219(S1):S88–96.
4.Human Vaccines & Immunotherapeutics. 2017, 13, 2837–2848.
5.Lancet. 2011; 378:360–68
6.Asian Pac J Trop Biomed. 2015; 5(5): 344-353.
7.Int J Mol Sci. 2018, 19, 3605.
8.Nature Reviews Drug Discovery. 2018, 17,261 - 279.
9.Clin Exp Vaccine Res. 2013;2:97-105.
10. Nature Medicine. 2005, 11, 683 - 689.
作者简介:
Enron Medicine是一个初入职场的医药人,读博期间养成了阅读文献的习惯,手上做的是化学,脑子里想的是信号通路,说出来的都是前人的足迹。希望有生之年可以做出让老百姓用得起的好药。
 总第1003期访问研发客网站可浏览更多文章www.PharmaDJ.com
总第1003期访问研发客网站可浏览更多文章www.PharmaDJ.com











