新冠病毒如何感染细胞?Delta为何这么毒?|《自然》长文
研究人员正在努力剖析新冠病毒的生命周期,看看它有哪些逃逸免疫系统的招数。
新冠病毒(SARS-CoV-2)有着很不一般的“糖衣”。“太惊人了。”Rommie Amaro盯着她为新冠病毒标志性刺突蛋白做的计算机模拟说道。这些刺突蛋白从新冠病毒的表面突起,包裹在聚糖(glycan)这种糖分子里。
“如果它包裹在这些聚糖中,那几乎就无法识别。”加州大学圣迭戈分校的计算生物物理化学家Amaro说。

为了伪装,许多病毒都会用聚糖包裹表面蛋白,就像披着羊皮的狼,逃过人体免疫系统的监视。去年,Amaro的实验小组与合作者基于结构和遗传学数据,利用超级计算机进行逐原子渲染,对这层“羊皮”进行了迄今精度最高的可视化。2020年3月22日,她在推特上发布了模拟结果。还不到一个小时,一位研究人员在评论中问道,从刺突蛋白顶部突出的无包裹裸露环状结构是什么?
Amaro被问倒了。但10分钟后,得克萨斯大学奥斯汀分校的结构生物数学家Jason McLellan回复道,这个裸露的环状结构是一个受体结合结构域(RBD),是刺突蛋白与人细胞表面受体结合的三个区域之一(见“藏起来的刺突蛋白”)。
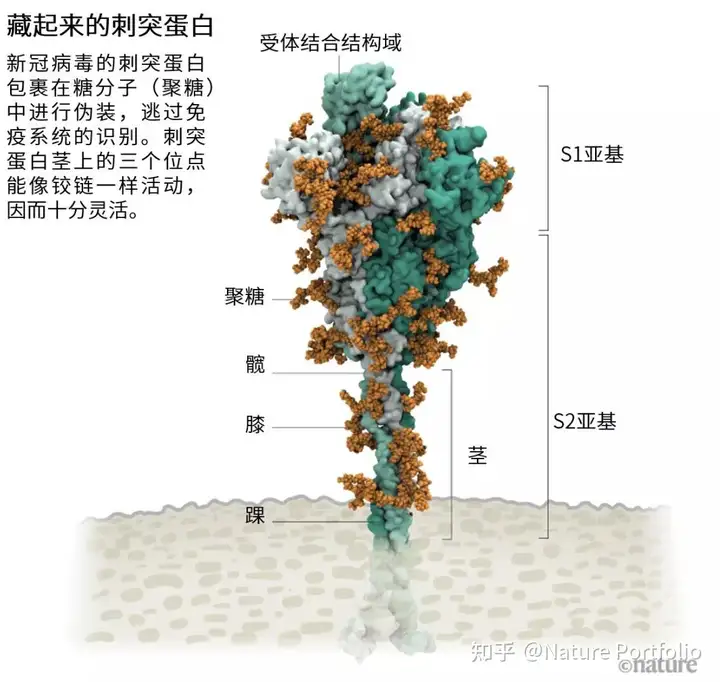
在Amaro的模拟中,当RBD上升到这团聚糖的顶部时,两个聚糖会突然将其锁住,就像自行车的撑脚架一样。如果Amaro改变计算机模型中的聚糖,RBD就会倒塌。McLellan的团队设法在实验室进行了同样的实验。到2020年6月,这些合作者已经报道称,改变这两个聚糖会降低刺突蛋白与人细胞受体的结合力[1]——之前从未在冠状病毒中发现过这种作用,McLellan说。剪掉这两个聚糖或能降低新冠病毒的感染性,Amaro说,可惜研究人员尚未找到这么做的方法。
自新冠疫情出现以来,研究人员已经对该病毒如何感染细胞有了详尽的认识。通过解析整个感染过程,研究人员希望凭借改良的疗法或疫苗抑制感染,同时搞清楚Delta等最新毒株的传播力为何会上升。
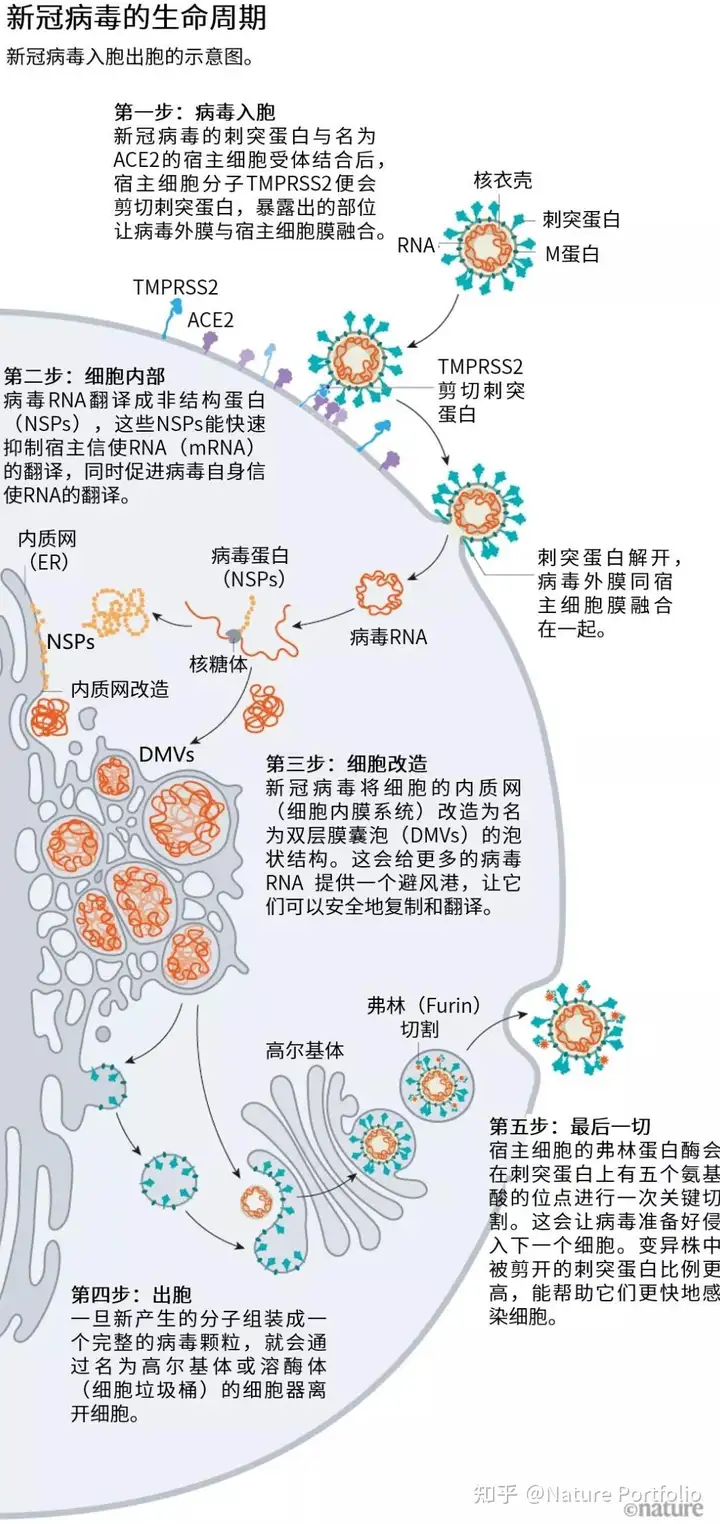
过去19个月的不懈努力,加之数十年的冠状病毒研究,我们正逐渐解开新冠病毒是如何一步步侵入人体细胞的(见“新冠病毒的生命周期”)。研究人员确定了新冠病毒能以出人意料的力量抓住人体细胞,而后立即遁形的关键适应机制。随后,新冠病毒离开细胞时又会使出关键一招,令其病毒颗粒能继续感染更多人体细胞。这是新冠病毒用来迅速传播、夺人性命的一些招数。帝国理工学院病毒学家Wendy Barclay说:“这是新冠病毒难以遏制的原因。”
蓄“刺”待发
一切从刺突蛋白开始。每个新冠病毒颗粒(virion)的表面有24-40个任意排列的刺突蛋白,这些刺突蛋白是病毒与人细胞融合的关键[2]。与流感病毒等其他病毒表面的刚性融合蛋白相比,新冠病毒的刺突蛋白非常灵活,能在三个点像铰链一样活动,德国马克斯·普朗克生物物理学研究所生物化学家Martin Beck和同事在2020年8月发表的一项研究中指出[3]。
如此一来,刺突蛋白就能任意掉头、摇摆、转动,这有利于它对细胞表面进行扫视,或是用多个刺突蛋白与一个人体细胞相结合。目前其他冠状病毒尚无类似实验数据,但由于刺突蛋白序列在演化上高度保守,可以推测所有冠状病毒都具有这一特点,Beck说。
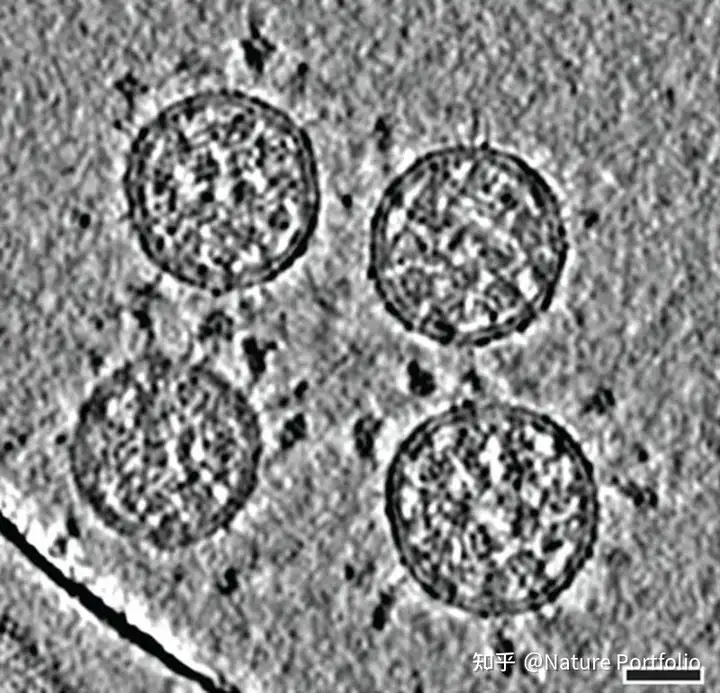
研究人员在疫情早期就证实了新冠病毒刺突蛋白的RBD能与ACE2受体结合。ACE2受体是一种常见的蛋白,广泛分布于人类喉部和肺部的大部分细胞表面。这个受体还是导致严重急性呼吸系统综合征的SARS病毒(SARS-CoV)的入胞点。但是,新冠病毒与ACE2的亲和力更好,估计是SARS病毒的2-4倍[4],这是因为RBD的多种变化能稳定其与病毒结合的热点位置[5]。
危险的新冠病毒变异株容易在刺突蛋白的S1亚基上携带突变,S1亚基包含RBD,并负责病毒与ACE2受体的结合(刺突蛋白的S2亚基则能促进病毒外膜与宿主细胞膜的融合。)
以Alpha变异株为例,它在刺突蛋白序列上有10个突变,导致RBD更有可能保持“向上”的状态[6]。“这能让病毒更易进入细胞。”美国北卡罗来纳州杜克人类疫苗研究所的结构生物学家Priyamvada Acharya说。Acharya正在研究刺突蛋白的突变。
目前Delta变异株正在世界各地传播,它在S1亚基上有多个突变,包括RBD上的3个突变,这3个突变似乎不仅能提高RBD与ACE2的亲和力,还能提高其逃逸免疫系统的能力[7]。
限定入口
病毒刺突蛋白与ACE2结合后,宿主细胞表面的其他蛋白就会启动病毒外膜与细胞膜融合的过程(见“病毒入胞近景”)。
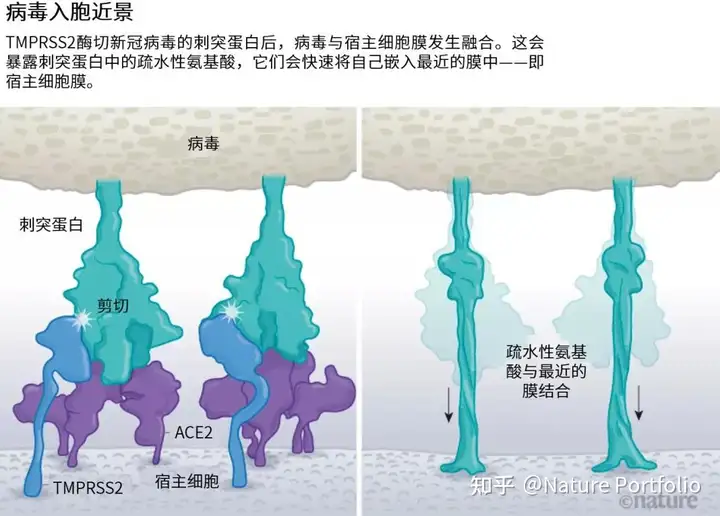
SARS病毒会利用两个宿主蛋白酶中的一个入胞:TMPRSS2(读作tempress two)或组织蛋白酶L。TMPRSS2的入胞途径更快,但SARS病毒经常通过核内体侵入,核内体是一种脂质包裹的囊泡,这个途径依赖组织蛋白酶L。不过,如果病毒颗粒从这一途径进入,就会被抗病毒蛋白逮个正着。
新冠病毒之所以不同于SARS病毒,就在于它能更快地利用TMPRSS2。TMPRSS2是呼吸道细胞表面大量存在的一种酶。TMPRSS2会先酶切刺突蛋白S2亚基上的一个位点[8]。这个剪切点会暴露一串疏水性氨基酸,暴露后的疏水性氨基酸会迅速嵌入最近的膜中——即宿主细胞膜。随后,展开的刺突蛋白会折叠起来,像拉链一样,迫使病毒外膜与细胞膜融合。
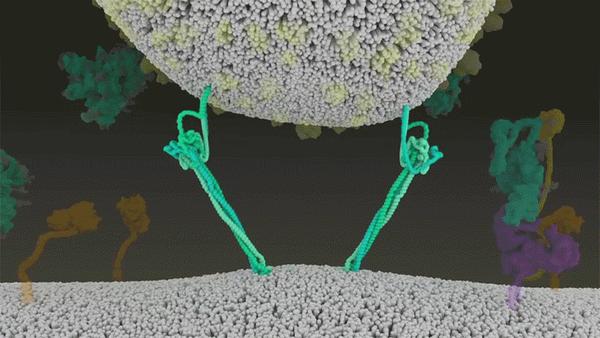
随后,新冠病毒将基因组直接注射到宿主细胞内。通过采取这种弹簧式的侵入方式,新冠病毒比SARS病毒的感染更快,而且不会被核内体逮住,Barclay和她在英国帝国理工学院的同事在4月发表的一项研究中描述道[9]。
新冠病毒能利用TMPRSS2实现快速入胞,解释了为何疟疾药物氯喹一开始在实验室研究中表现良好,但在治疗COVID-19的临床试验中无效[10]。原来氯喹利用的细胞完全依赖组织蛋白酶实现核内体侵入。“新冠病毒在人类气道中传播和复制时不会用到核内体,所以氯喹这种核内体干扰药物在真实人体中效果就不大了。”Barclay说。
这一发现还指出,蛋白酶抑制剂是一种很有希望的治疗选项,可以防止病毒利用TMPRSS2、组织蛋白酶L或其他蛋白酶进入宿主细胞。camostat mesylate是一种TMPRSS2抑制剂,日本已将其批准用于治疗胰腺炎。这种抑制剂能阻断病毒进入肺部细胞[8],但无法在初步临床试验中提高病人的治疗转归[11]。
“依我看,我们应当将这种蛋白酶抑制剂作为广谱抗病毒药物,防止新的疾病发展为大流行,将其遏制在萌芽阶段。”德国灵长类研究中心感染生物学部主任Stefan Pöhlmann说。Pöhlmann领导开展了ACE2结合和TMPRSS2途径的研究。
致命竞争
接下来的感染步骤就没那么清晰了。“进入细胞之后就有很多黑箱。不确定性和各种假说也更多了。”美国犹他大学的化学家Janet Iwasa说。Iwasa正在制作一个解释新冠病毒生命周期的带注释的动画。
就在新冠病毒将RNA基因组注射到宿主细胞后,细胞质核糖体会将两个病毒RNA片段翻译成氨基酸长链,这些氨基酸长链再被切割出16个蛋白质,包括许多参与RNA合成的蛋白质。随后会产生更多的RNA,这些RNA编码26个已知的病毒蛋白,包括用来制造新病毒颗粒的结构蛋白(比如刺突蛋白)和其他协助蛋白。这样,病毒就能大量产生其自身的信使RNA(mRNA)拷贝,但它还需要细胞机器来将这些mRNA翻译成蛋白质。
新冠病毒有很多将细胞机器占为己用的策略。病毒学家Noam Stern-Ginossar和她在以色列魏茨曼科学研究所的团队重点研究了新冠病毒抑制宿主mRNA翻译、促进自身mRNA翻译的三种机制。虽然这三种机制并非新冠病毒所独有,但这些作用的结合、速度和程度看来确实是独一无二的,Stern-Ginossar说。
第一,新冠病毒会清除竞争对手:病毒蛋白Nsp1是新冠病毒抵达时首先被翻译的蛋白之一,它会把宿主蛋白质招募起来,系统性地切割所有不带病毒标记的细胞mRNA。如果Stern-Ginossar的团队将同样的病毒标记放在宿主mRNA的末端,这个mRNA就不会被切割[12]。
第二,感染会让细胞内全部蛋白质翻译减少70%。Nsp1依然是捣蛋分子,这一次它能阻断核糖体的入胞渠道,让mRNA无法进入,两个研究团队分别得出了以上结论[13,14]。剩下不多的翻译能力全被用来翻译病毒RNA,Stern-Ginossar说。
第三,新冠病毒会关闭细胞的预警系统。这有很多方式,但Stern-Ginossar的团队发现了新冠病毒的一个明确机制:病毒让细胞mRNA无法离开细胞核,包括提醒免疫系统注意感染的蛋白质的指令。另一个团队证实了这个结果,再次将矛头指向Nsp1:这个蛋白似乎会阻塞离开细胞核的通道,一个不让逃走[15]。
由于基因转录本无法离开细胞核,因此受感染的细胞不会释放许多干扰素——干扰素是提醒免疫系统注意病毒的信号蛋白。新冠病毒关闭这一预警系统的速度尤其快:和其他呼吸道病毒相比,包括SARS病毒和呼吸道合胞病毒,新冠病毒感染后诱导的干扰素水平显著降低[16]。今年6月,研究人员报道了Alpha变异株的突变似乎能更有快地减少干扰素的产生[17]。
“新冠病毒明显是个动作很快的病毒,具有非常独特的能力,能从源头上扰乱免疫系统识别病毒和抵抗感染的能力。”Stern-Ginossar说。等到免疫系统真正发现有病毒时,病毒数量已经太多了,致使免疫应答蛋白有时会比平常更快地充斥在血液中,而这可能对人体有害。临床医生在疫情很早就发现,有些发展成重症的COVID-19患者除了受到病毒本身的袭击外,过度激活的免疫应答也造成了一定伤害。一些经证明有效的疗法专门抑制这种免疫应答。
最强改造王
新冠病毒接管宿主细胞翻译后,它就开始喧宾夺主了,朝着有利自己的方向大肆改造细胞内部和表面。
首先,一些新制造的刺突蛋白会抵达宿主细胞表面,突破宿主细胞膜。它们还会在那里激活一条宿主钙离子通道,在细胞表面分泌一层脂肪膜——肌肉细胞等自然融合的细胞上也会发现这种膜。这时,受感染细胞与表达ACE2的相邻细胞融合,发展为最多包含20个细胞核的单个大呼吸道细胞。
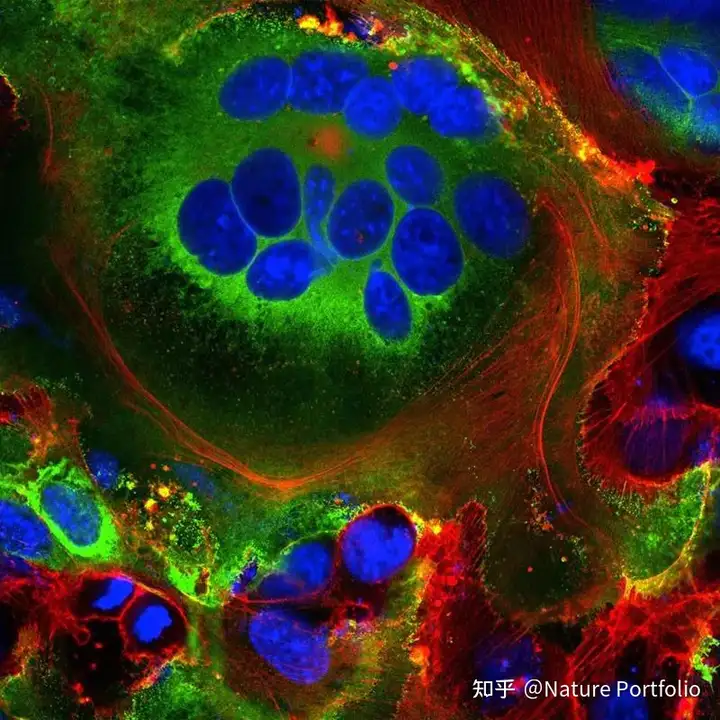
这些融合结构被称为合胞体(syncytia),HIV和单纯疱疹病毒等病毒感染会诱导形成合胞体,但SARS病毒就不会,伦敦国王学院的分子生物学家Mauro Giacca说。Giacca领导的团队在4月发表了这项研究结果[18]。他的假设是,形成合胞体能让受感染细胞存活更长时间,制造更多病毒颗粒。“这不是一个会肇事逃逸的病毒。”他说。“它会一直存在。”中国医学科学院研究员孙强领导的另一支团队发现,新冠病毒感染的一些细胞甚至会与淋巴细胞形成合胞体,淋巴细胞是人体自身的免疫细胞[19]。这其实是肿瘤细胞的免疫逃逸机制,而非病毒的机制,提示我们受感染细胞会抓住周围的免疫细胞并与之融合,轻而易举地逃过免疫系统的侦查。
细胞内部的变化就更多了。内质网(ER)是参与蛋白合成与转运的平面膜系统,和其他冠状病毒一样,新冠病毒会将又长又细的内质网变成一个具有双层膜的球体,就好像内质网在吹泡泡一样。这些双层膜囊泡(DMVs)或许能为病毒RNA提供一个复制和翻译的避风港,保护其不被细胞内的天然免疫传感器发现。当然,这个假说仍有待验证。
参与制造DMVs的蛋白或许是很好的药物靶点,因为它们对病毒复制好像起着不可或缺的作用。比如,TMEM41B这种宿主蛋白必须被用来调动胆固醇和其他脂质来扩大内质网膜,以便所有病毒成分都能进入其中[20]。“把TMEM41B拿走会对感染产生很大影响。”参与这项研究的得克萨斯大学医学部的新冠病毒研究员Vineet Menachery说。此外,新冠病毒跨膜蛋白Nsp3也可作为药物靶点:它会在DMVs上形成冠状孔,将制造好的病毒RNA转运出去[21]。
大部分具有外层膜(即包膜)的病毒获得这一特征的方式是直接在细胞边缘组装,并在离开的路上选择一些细胞自己的质膜。但新制造好的冠状病毒蛋白会选择另一个途径。
多年来的证据已经表明,冠状病毒会通过高尔基复合体转出细胞。高尔基复合体是具有邮局功能的细胞器,能将分子包在膜内,运送至细胞其他部位。病毒会在那里从高尔基体膜形成一个脂质包膜;新形成的病毒颗粒再在高尔基囊泡中转运到细胞表面,并分泌到胞外,美国约翰斯·霍普金斯大学病毒学家、生物学家Carolyn Machamer说。Machamer研究冠状病毒已经有30年了。
但在去年12月,美国国家心脏、肺和血液研究所的细胞生物学家Nihal Altan-Bonnet和她的同事报道,他们发现了冠状病毒会通过溶酶体离开细胞——溶酶体是细胞的垃圾桶,拥有很多能分解细胞成分的酶[22]。阻断基于高尔基体的分泌途径似乎不会影响释放的感染病毒数量,Altan-Bonnet说。她团队的证据[22]显示,病毒蛋白在内质网出芽形成包膜,再占用溶酶体离开细胞。目前,该团队正在检测阻断溶酶体出胞过程的抑制剂是否能成为潜在的抗病毒药物。
无论是通过高尔基体还是溶酶体离开细胞,都比通过质膜出芽要慢、效率也更低,所以研究人员不明白新冠病毒为什么会这么做。Machamer推测,相比质膜,来自高尔基体或溶酶体的包膜的脂质组成好像对新冠病毒更有利。“如果我们能更好地理解这个部分,就有很大的机会找到新的抗病毒疗法。”她说。
最后一切
在离开细胞时,还有一步让这个病毒成为传染王:在有5个氨基酸的位点进行快速切割能让该病毒准备好攻击下一个目标。
其他冠状病毒在刺突蛋白S1和S2亚基的连接处只有一个精氨酸,新冠病毒却有5个连着的氨基酸:脯氨酸、精氨酸、精氨酸、丙氨酸、精氨酸。“由于这个位点非常特殊,我们就盯着它,最后发现这个位点确实是侵入肺部细胞的关键。”Pöhlmann说。2020年5月,他和同事报道了名为弗林(furin)的宿主细胞蛋白能识别并切割这个氨基酸链,而且这种切割对于新冠病毒快速进入人肺部细胞是“至关重要的”[23]。
这不是研究人员第一次在病毒上发现弗林切割位点;致病性很高的禽流感病毒也有这个位点,Barclay说。当一位同事把培养的自然失去弗林切割位点的新冠病毒变异株给到Barclay时,她的团队发现感染该毒株的雪貂比感染大流行毒株的雪貂脱落的病毒颗粒更少,而且不会将病毒传给周围的动物[9]。正当Barclay的团队准备在2020年9月的预印本论文中报道该结果时,荷兰的一项研究也发现,拥有完整弗林切割位点的冠状病毒进入人气道细胞的速度比没有弗林切割位点的更快[24]。
研究人员推测弗林会在病毒颗粒组装过程中或是释放前切割该位点。这个时间点解释了新冠病毒为何会通过高尔基体或溶酶体离开细胞,芝加哥洛约拉大学的病毒学家Tom Gallagher说。“这个病毒一经组装就会移动到周围都是弗林蛋白酶的细胞器中。”
通过剪切S1和S2亚基之间的连接键,弗林酶切让病毒颗粒的刺突蛋白松开,以便它们在进入细胞时对TMPRSS2的二次切割产生反应,这次切割暴露出的疏水性区域会快速将自己嵌入宿主细胞膜内,Gallagher说。如果刺突蛋白没有被弗林蛋白预先切开——有时也不会被切开——它们就会绕开TMPRSS2,通过更慢的核内体途径进入细胞,或是根本不进入细胞。
Alpha和Delta变异株的弗林切割位点都发生了变化。Alpha变异株将本来的脯氨酸替换成组氨酸(P681H);Delta变异株则替换成了精氨酸(P681R)。这两个变化都会减少序列的酸性;而且氨基酸链碱性越强,它们被弗林识别切割的效果也更好,Barclay说。“我们的假设是,这体现出新冠病毒的传递能力增强了。”
更多弗林酶切意味着更多刺突蛋白准备好进入人体细胞。SARS病毒只有不到10%的刺突蛋白做好了这种准备,Menachery说。Menachery的实验小组一直在量化这些做好准备的刺突蛋白,但研究成果尚未发表。对新冠病毒来说,这个比例上升至50%,而Alpha毒株超过了50%,该团队发现,在传染性很强的Delta毒株中,75%以上的刺突蛋白准备好继续感染人体细胞。
走向未知
科研界其实才刚刚开始理解新冠病毒。一些关键的未知数还包括:与每个刺突蛋白结合所需的ACE2受体数量;S2位点究竟是何时被TMPRSS2切割的;病毒外膜与细胞膜融合所需的刺突蛋白数量,McLellan说,而这些还只是入胞的问题。2020年4月,加州大学旧金山分校的一个团队鉴定出了新冠病毒与人类蛋白质相互作用的至少332种方式[25]。
想要赶上这个快速变异的病毒很不容易。但专家一致认为,迄今发现的主要是变异与病毒传播速度的相关性,而不是与病毒对宿主伤害的相关性。7月的一项研究报道,Delta变异株在肺部和喉部的生长速度比之前的变异株快很多[26]。
但是,现在还不确定Delta携带的突变如何以这种方式为其毒力加码,Stern-Ginossar说,“许多实验室正在竭力回答这些问题。”
参考文献:
1. Casalino, L. et al. ACS Cent. Sci. 6, 1722–1734 (2020).
2. Ke, Z. et al. Nature 588, 498–502 (2020).
3. Turoňová, B. et al. Science 370, 203–208 (2020).
4. Nguyen, H. L. et al. J. Phys. Chem. B 124, 7336–7347 (2020).
5. Shang, J. et al. Nature 581, 221–224 (2020).
6. Gobeil, S. M.-C. et al. Science https://doi.org/10.1126/science.abi6226 (2021).
7. Khateeb, J., Li, Y. & Zhang, H. Crit. Care 25, 244 (2021).
8. Hoffmann, M. et al. Cell 181, 271–280 (2020).
9. Peacock, T. P. et al. Nature Microbiol. 6, 899–909 (2021).
10. Wang, M. et al. Cell Res. 30, 269–271 (2020).
11. Gunst, J. D. et al. EClinicalMedicine 35, 100894 (2021).
12. Finkel, Y. et al. Nature 594, 240–245 (2021).
13. Schubert, K. et al. Nature Struct. Mol. Biol. 27, 959–966 (2020).
14. Thoms, M. et al. Science 369, 1249–1255 (2020).
15. Zhang, K. et al. Sci. Adv. 7, eabe7386 (2021).
16. Blanco-Melo, D. et al. Cell 181, 1036–1045 (2020).
17. Thorne, L. G. et al. Preprint at bioRxivhttps://doi.org/10.1101/2021.06.06.446826 (2021).
18. Braga, L. et al. Nature 594, 88–93 (2021).
19. Zhang, Z. et al. Cell Death Differ. https://doi.org/10.1038/s41418-021-00782-3 (2021).
20. Trimarco, J. D. et al. PLoS Pathog. 17, e1009599 (2021).
21. Wolff, G. et al. Science 369, 1395–1398 (2020).
22. Ghosh, S. et al. Cell 183, 1520–1535 (2020).
23. Hoffmann, M., Kleine-Weber, H. & Pöhlmann, S. Mol. Cell 78, 779–784 (2020).
24. Mykytyn, A. Z. et al. eLife 10, e64508 (2021).
25. Gordon, D. E. et al. Nature 583, 459–468 (2020).
26. Li, B. et al. Preprint at medRxiv https://doi.org/10.1101/2021.07.07.21260122 (2021).
原文以How the coronavirus infects cells — and why Delta is so dangerous标题发表在2021年7月28日的《自然》的新闻特写版块上
原文作者:Megan Scudellari
头图来源:Mauro Giacca
© nature
doi: 10.1038/d41586-021-02039-y
版权声明:
本文由施普林格·自然上海办公室负责翻译。中文内容仅供参考,一切内容以英文原版为准。欢迎转发至朋友圈,如需转载,请邮件China@nature.com。未经授权的翻译是侵权行为,版权方将保留追究法律责任的权利。
© 2021 Springer Nature Limited. All Rights Reserved
本站所有文章、数据、图片均来自互联网,一切版权均归源网站或源作者所有。
如果侵犯了你的权益请来信告知我们删除。邮箱:dacesmiling@qq.com